锂电黑科技:无负极锂电池稳定运行1066小时
一、无负极二次锂金属电池设计的方式及关键点
随着储能行业的不断发展,追求更高能量密度、更低成本、更安全、更稳定的锂电池已势不可挡。尽管目前以石墨为负极的锂离子电池(LIBs)在电子设备、电动汽车和智能电网存储领域颇受重视,但其较低的能量密度明显跟不上日益增长的使用需求。因此,锂金属负极又重回舞台,以取代石墨负极,为电池提供更高的能量密度。锂金属负极的理论比容量为3820 mA h/g,是石墨负极的10倍(372 mA h/g)。然而,锂金属负极在工作的时候,常常伴随着锂的均匀沉积、以及形成不稳定的固体电解质界面层(SEI),导致锂在电镀/剥离后生长大量的枝晶,引发电池的安全问题,缩短电池寿命。因此,如何避免以上问题,在增加能量密度的同时提高电池安全性能,是研究者们正在思考的新命题。
其中一个很新颖的想法是使用Anode-Free系统。原则上,如果从正极中脱出的锂离子,可以可逆地在铜集流体上进行电镀和剥离,则可以组装出Cu/隔膜/正极/Al型的可充电锂金属电池。由于这种电池中没有活性负极,因此被称为“无负极可充电锂金属电池”(AFLMB)。这里的“无负极”并不是说电池中真的没有负极,而指的是无负极活性物质作为Li+的宿主。因此,这种设计可以减少电池的重量和空间,与传统锂离子电池相比,AFLMB的能量密度将显著提升。如果该类型的电池能进入工业,那将节省与负极生产(包括浆料制备、浆料涂层和干燥)工序相关的成本和时间。然而,除了上述优点外,AFLMB有一个致命的缺点,那就是其SEI非常不稳定,因此会消耗大量的活性锂和电解质,因此库仑效率(CE)和循环容量保留率较低。
在这类无负极电池系统中实现稳定的锂电镀/剥离过程,其关键在于设计出性能更好的电解质。而设计电解质时,首先应考虑锂盐的选择、溶剂和浓度的控制。固体电解质、无机电解质以及混合离子液体电解质虽然可以抑制锂枝晶生长,但其在室温下具有低导电性和高界面电阻,动力学性能受到很大限制。传统锂离子电池中采用的电解质为1 M LiPF6,电解液为碳酸盐基溶剂,然而碳酸盐电解质体系与锂金属的相容性较差,极易导致锂枝晶生长,因此也不能用在AFLMB中。近来,Zhang等人采用一种高浓度的醚基电解质(4 M LiFSI/DME)来稳定锂负极(Nat. Commun. 2015, 6, 6362)。的确,高浓度电解质可以提高正负极氧化物的稳定性、无游离溶剂、高阴离子含量、提高活性锂离子数量。然而,醚基溶剂的抗氧化能力较差且成本高,无法满足高压正极的稳定运行,因此实用性不高。如果从成本角度考虑,六氟磷酸锂(LiPF6)无疑是最好的选择。
二、如何设计电解液组成来稳定电化学循环
国立台湾科技大学Bing-Joe Hwang等人采用高浓度LiPF6 in EC/DEC(1:1 v/v)电解液,搭配50%的氟乙烯碳酸盐(FEC)稀释剂,将NMC//Cu这种无负极锂金属电池的循环寿命提高到1066小时以上。
1.探究电解液浓度对电池稳定性的影响
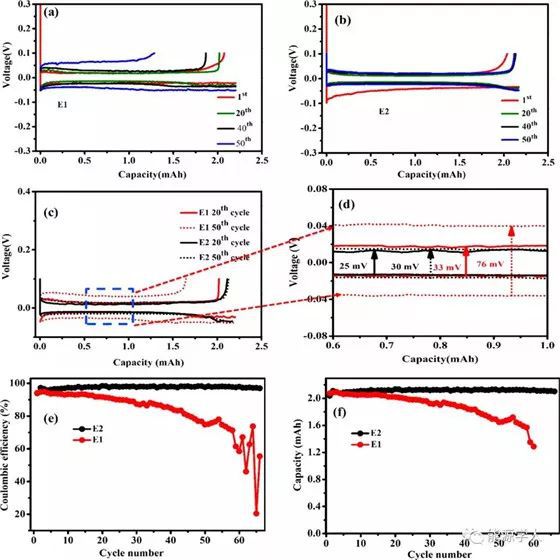
为了理解电池的极化、循环、库伦效率,作者首先进行了Li||Cu半电池测试。上图中E1.5表示1.5 M LiPF6,E2表示2 M LiPF6,E3表示3 M LiPF6,E4表示4 M LiPF6。从循环的CE中,可以理解锂电镀/剥离过程中的活性锂的消耗速率、及电解质的分解程度。E1和E2情况下的电池在0.2mA/cm2电流密度下的CE趋势如上图e所示,由于半电池中的负极为锂箔,则CE的本质为由于电解质分解而导致铜集流体上的锂损耗。在图e中,E1和E2在一开始时的库伦效率均为~94%,这表明,无论电解质类型和浓度如何,电池的第一个循环中几乎没有什么差异。然而,在含有E1电解质的电池中,CE衰减很快,仅仅几个循环,就开始出现波动。同样的趋势从图c和图d中也可看出,仅仅50个循环,E1电池的极化电压就升高至76 mV,这表明,在经过几个电镀/剥离循环后,E1电池中的死锂沉积较厚,从而在铜表面快速生长锂枝晶,导致高电阻层的形成,增大离子和电子扩散电阻,从而使极化电压迅速上升。上述这种现象也再一次证明了商业1 M LiPF6 EC/DEC 1:1 v/v电解质于AFLMB不兼容。与之对比,E2电池可以稳定循环超过1066h,CE一直维持在98%,极化电压仅为30 mV,首次循环的极化率很高,第二次循环后极化率下降,这说明由高浓度电解质E2可以形成更加稳定的SEI。作者将性能优异的原因归功于FEC稀释剂和高浓度电解质中的盐协同作用,形成坚固的SEI,防止锂枝晶的形成。
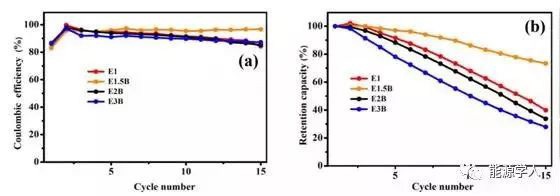
上图为无负极Cu ‖ NMC纽扣电池在0.2 mA/cm2下运行时,不同浓度电解质的库伦效率和容量保留率对比(B表示不含FEC稀释剂)。
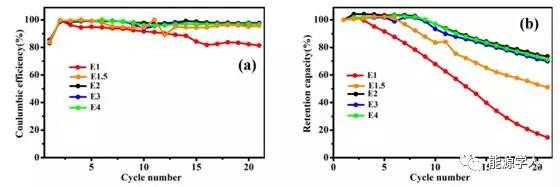
上图为无负极Cu ‖ NMC纽扣电池在0.2 mA/cm2下运行时,不同浓度电解质的库伦效率和容量保留率对比(含有FEC稀释剂)。
三、铜负极表面SEI的分析,探究电池能循环稳定的原因
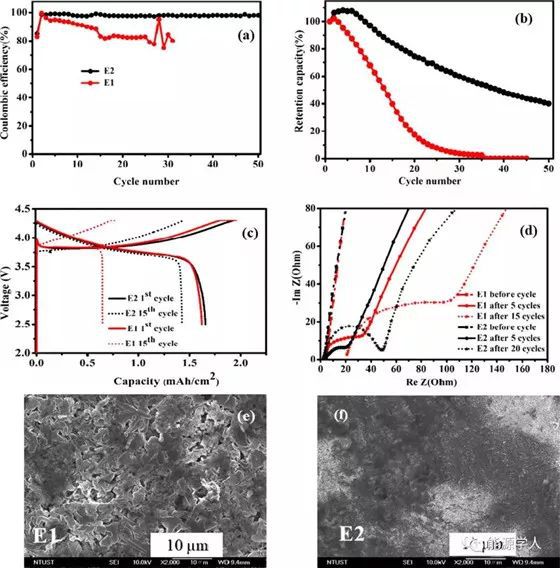
无负极Cu||NMC纽扣电池正极为NMC111,负极为Cu箔,电解液为不同浓度的LiPF6 in EC/DEC (1:1 v/v ratio),以FEC为稀释剂。即便有文献显示碳酸盐溶剂(EC/EMC (3:7 wt %)在第一次充电后会损失77%(J. Electrochem. Soc. 2014, 161, A827?A830.),作者的实验还是表示,不管电解质类型如何,在AFLMB首次循环中,电解液损失几乎只有14%。但是15圈以后,E1电解质的损耗高达60%(上图c)。如上图a所示,使用E1电解质的AFLMB电池,其CE迅速下降(<90%),几个循环后开始波动,这可能由于在连续电镀/剥离过程中,游离溶剂与活性锂离子反应导致活性锂耗尽。另外,传统碳酸盐电解质中形成的SEI层由电解质溶剂分解而成,因此消耗电解质也是另一个原因。
相反,如上图b,c所示,高浓度电解质E2即使在第15个循环时,CE仍保持在86%以上。如图2b所示,即使经过50个循环,ACE仍超过97.8%,这是目前已知的碳酸盐基溶剂在AFLMB中的最高值。为了进一步了解高浓度LiPF6和FEC稀释剂的协同作用对稳定无负极电池的正面影响,作者采用电化学阻抗谱(EIS)研究了电解质/电极界面行为。从上图d也可以看出,含有E1的电池,在15个循环期间,电阻非常高,这表明与死锂反应的SEI很厚,增加电子和离子扩散电阻。从上图e中的扫描电镜形貌也很容易的观察到死锂粉体。然而,即使经过20个循环,带有E2电解质的电池明显电阻较低,这显然证明了稀释剂具有通过降低粘度来提高离子导电性的作用。
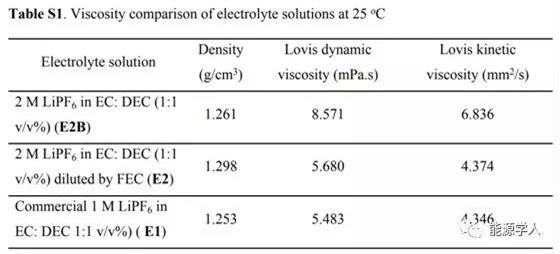
在上表中可以观察到电解液的粘度对比,高浓度E2B电解质的Lovis动态粘度为8.571mPa·s,高于加入稀释剂厚的E2电解质(5.680mPa·s)。
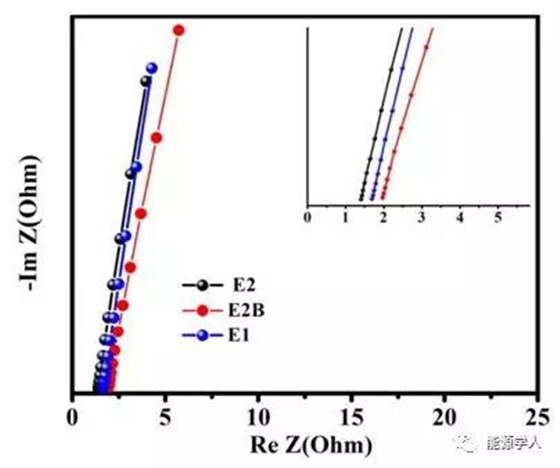
通过对比不锈钢、不锈钢电池的阻抗,可以看出不同电解液的离子导电性,如上图所示。

电解质的离子电导率是根据电阻(R)数据计算得出的,如上式所示,R表示电解质溶液的电阻,ρ表示电阻率,L表示两个电极之间的距离,A表示横截面积。因此,溶液的离子电导率k与电阻率(ρ)的倒数有关。计算得到高浓度电解质E2的离子导电率为1.34×10-3 s cm-1,高于E1 (1.12×10-3 s cm-1),高于E2B (9.54 × 10–4 S cm–1)。
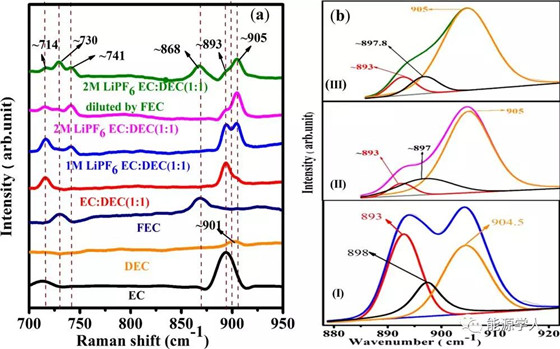
一般来说,稀释剂的作用主要是降低粘度和增加电导率,但由于离子对的电荷中性,其对高浓度电解液的离子迁移率并没有很大影响。它不会改变高浓度电解质的特性,因此SEI的形成主要是由溶剂化盐络合物的分解产物组成。上图a中位于714 cm-1处的拉曼特征峰,属于EC中的C═O弯曲振动;随着LiPF6浓度的增加,其强度逐渐降低,并向741 cm-1处移动,这是PF6–的特征峰。同样,在图a中还出现了位于893 cm–1处的EC分子特征峰,随着LiPF6浓度的增加,该峰逐渐被905 cm–1处取代,但这仍旧属于EC分子的特征峰。这表示FEC是良好的稀释剂,即使由于溶液中存在FEC而出现新的峰,但溶液结构仍不受稀释剂的影响。因此,由于稀释剂不影响溶液溶剂化结构的特性,SEI的形成机理仍旧主要是由阴离子的分解产物所决定的,与市售电解质E1相比,高浓度电解质中游离溶剂的量明显减少。此外,从图b (I–III)的拟合曲线来看,随着盐浓度的增加,位于893cm-1处的自由溶剂EC峰强度逐渐减小,并向更高的波段移动。
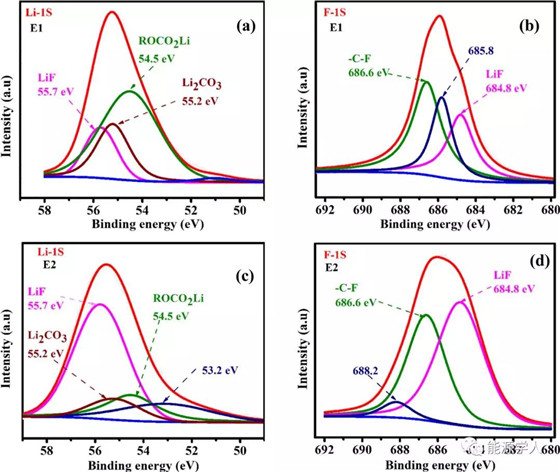
为了更好的了解铜负极表面SEI的化学成分,作者对5个循环后完全放电的负极进行XPS表征。上图a-d分别显示了使用E1电解质的Li-1s、使用E1电解质的F-1s、使用E2电解质的Li-1s和使用E2电解质的F-1s XPS特征峰。图a、c所示的Li-1s光谱中,55.2、55.4和55.7eV处的峰分别属于Li2CO3、ROCO2Li和LiF。同样的,图b、d所示的F-1s光谱中,684.8和686.6 eV处的峰分别属于LiF和C–F。但是,也有一些峰尚未对应特定的化合物或官能团,例如L-1s中的53.2 eV(图c)、使用E2电解质的F-1s中的688.2 eV(图d)和使用E1电解质的F-1s中的685.8 eV(图4b)。在图a的光谱中,使用E1电解质,可以明显地观察到,有机物的峰值强度很高,例如在Li-1s光谱中的ROCO2Li和在O-1s和C-1s光谱中的?CH2–CH2O, C═O,表明SEI的主要成分来自溶剂分解。而在高浓度E2电解质中,SEI膜中含有无机物(如LiF)的高峰值强度。图c,d中LiF光谱强度的增加可能是由盐分解引起的阴离子一次还原,这是阴离子衍生SEI形成的证据。一般来说,在高浓度E2电解质的SEI膜组成中,其他无机物如Li2O和Li2CO3也支持这一证据。
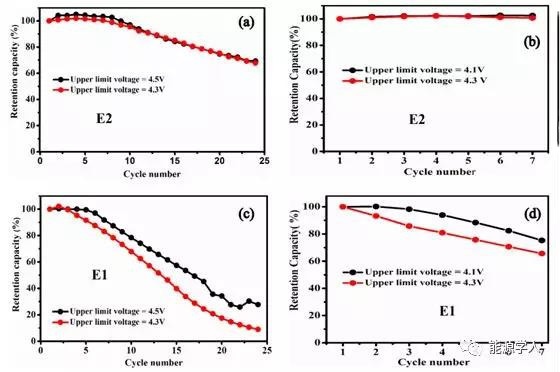
此外,作者还研究了高浓度电解质对不同上限电压的稳定性。可以看出,当上限截止电压从4.3 V变为4.1 V和从4.3 V变为4.5 V时,E1电解质的放电容量有显著差异,如上图c,d所示。截止电压上限越低,保留容量越高,这与理论预期相符。然而,在高浓度电解质中,无论上述电压变化之间的变化如何,保留容量几乎保持不变,如图a,b所示,这表示高浓度电解质在高电压下的稳定性更好。
结论:
1. 无负极锂金属电池(AFLMB)作为一种新颖的储能系统,尽管能量密度相对提高,但一直找不到适合的电解液。常见的高浓度醚类电解质不仅成本高,而且不能耐高压,因此急需找到一种低成本、高稳定性的电解质。在本文中,作者采用高浓度LiPF6 in EC/DEC(1:1 v/v)电解液,搭配50%的氟乙烯碳酸盐(FEC)稀释剂,将NMC||Cu这种无负极锂金属电池的循环寿命提高到1066小时以上。
2. 在Li||Cu半电池测试中,不论电解质的类型和浓度如何,电池的首次库伦效率均为~94%,但是,仅仅几个循环后,低浓度的电解质便开始快速衰减,无法稳定运行。此外,作者发现50个循环后,低浓度电解质的电池极化电压就升高至76 mV,这表明,在经过几个电镀/剥离循环后,低浓度电解质的电池中死锂沉积较厚,从而在铜表面快速生长锂枝晶,导致高电阻层的形成,增大离子和电子扩散电阻,从而使极化电压迅速上升。
3. 在无负极Cu||NMC纽扣电池测试中,使用E1电解质的AFLMB电池,其CE迅速下降(<90%),几个循环后开始波动,这可能由于在连续电镀/剥离过程中,游离溶剂与活性锂离子反应导致活性锂耗尽。另外,传统碳酸盐电解质中形成的SEI层由电解质溶剂分解而成,因此消耗电解质也是另一个原因,但高浓度的电解质就没有这个问题。
本文链接:https://www.nxebattery.com{dede:field.arcurl/}
诺信新闻,诺信公司新闻,锂电池行业新闻,展会新闻
下一篇:锂电池保护板IC方案介绍